介绍在构象分析的基础上,对杯[4]芳烃在酚氧原子(下环)和苯环(上环)上的不同功能化进行了超分子主-客体化学研究。[1,2]摘要制备了许多杯[4]芳烃下缘4个羟基的衍生物,研究了它们在金属和有机阳离子的结合和转运方面的功能和行为。(3 - 5) 在另一方面,膦酸酯,膦和氧化膦的衍生物已被公知作为用于金属离子有用提取剂[6]和/或作为在有机合成反应的过渡金属催化剂的有效配体。[7]因此,它是很有价值的和有用的开发新杯[4]芳烃拥有这些磷组较低的边缘直接引入苯环上,这可能会前所未有的特定功能和行为,包括运输和萃取剂的金属和有机阳离子,并在有机催化反应。 然而,只有合成报道杯[4]芳烃具有在低甲氧基组rim和两个diphenylphosphine氧化物,四膦酸酯[8],[9]或四个三苯基膦组[10]的直接取代的苯环上边缘,没有研究构象分析,功能和行为。众所周知,杯[4]芳烃的功能和行为在很大程度上受特征构象(锥形、部分锥形、1,2-交替或1,3-交替)和低边缘的一种取代基以及杯[4]的构象稳定性的影响在低边缘具有四个甲氧基的芳烃通常相对较低,难以表征。一些研究[11-14]还对杯[4]芳烃的化学进行了研究,杯[4]芳烃在上边缘具有四个膦酸盐或磷化氢基团,在这些基团和苯环之间具有一些功能取代基作为间隔基,尽管杯[4]芳烃含有四个羧酸盐[15,16]和磺酸盐基团[16,17]我们已经很出名了。 在这项研究中,我们希望报道多种新型杯[4]芳烃衍生物6-8的合成,其上边缘带有四个膦酸盐或氧化膦基团,下边缘带有四个烷基醚基团。此外,对这些化合物的构象分析和萃取行为的研究表明,具有四个二苯基氧化膦和丙氧基的杯[4]芳烃(6c-cone18)对FeCl的萃取具有较高的选择性和较高的能力3.. 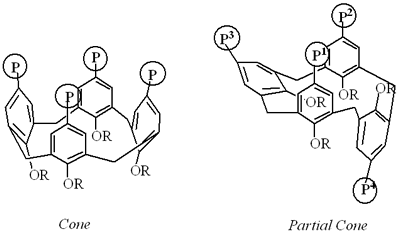
图1。锥体及部分锥体结构。 实验典型的程序的Arbuzov反应对于Tetrabromocalix的阿尔布佐夫反应的典型程序[4]芳烃衍生物1-4与亚磷酸酯或次膦酸酯 每个tetrabromocalix [4]芳烃的1-4 tetraalkylethers [16](1毫摩尔)在苄腈搅拌(8毫升)的二溴化镍(1毫摩尔)在180℃下存在。加入亚磷酸三烷基或二苯基磷酸乙酯(20 mmol)的苯腈(2ml)溶液,在180℃下搅拌30分钟。后的溶液冷却至室温,甲苯(100毫升)中的溶液,用5%-NH3.水溶液(100 ml x 2)和干燥(MgSO4.)。经过滤去除干燥剂后,用蒸馏法蒸发溶剂。残渣以丙酮为洗脱物,在硅胶上用闪速柱层析法进行纯化,得到的产物几乎是纯固体,如表1所示。所有产物为杯[4]芳烃衍生物,含有四个氧化二苯膦或四个二烷基膦酸酯5a, 6a-c, 7a-c和8a-c,通过光谱分析(IR, 1H-NMR, 13C-NMR, MASS)和元素分析进行表征,如下图所示。通过与真实样品光谱行为的比较,鉴定了杯[4]芳烃5b-c,其下缘有四个甲氧基,上缘有四个磷酸二丙酯或氧化二苯膦基。 5,11,17,23-四(二乙基膦酰基)-25,26,27,28-tetramethoxycalix [4]芳烃(5a)化合物: IR(纯的)1260(P = O);1 H-NMR(400MHz,CDCL3.)δ: 7.78 (d、2 h, J = 13.2赫兹,Ph值),7.58 (d, 2 h, J = 13.2赫兹,Ph值),7.43 (d, 2 h, J = 12.7赫兹,Ph值),7.00 (d, 2 h, J = 13.2赫兹,Ph值),4.39 - -3.16 (m, 8 h,拱门2.基于“增大化现实”技术,哟2.中国3.哟,3.),3.61(brs,3H,OCH3.), 3.19 (br、3 h,哟3.),1.41-1.26(M,15H,OCH2.中国3.), 1.18(t, 3H, J=7.0Hz, OCH2.中国3.), 1.03(brs, 6H, OCH2.中国3.);13 C-NMR(100MHz的,CDCL3.)δ: 161.1, 161.0, 160.9, 160.8(d, 4JPC=3.7Hz), 136.2, 136.1, 136.0, 134.7(d, 2JPC=9.2Hz), 133.9(d, 3JPC=14.7Hz), 133.5, 133.3, 132.9(d,2JPC=9.2Hz)、132.5(d,2JPC=11Hz)、132.3(d,2JPC=11.0Hz)、122.7、122.6、122.1、122.0、120.8、61.9、61.8、60.7、60.0、58.5、53.8、36.4、31.7、30.8、30.5、30.5、29.2、16.3、16.2、15.9(s)、用于计算肛门粘膜厚度:1025毫米48H68O16P4.: C, 56.25;6.69 H,。发现:C, 56.45;6.59 H,。 圆锥- 5,11,17,23 - tetrakis (diethylphosphono)- 25,26,27,28 -tetra-n-propoxy杯[4]芳烃[6a]: m、 p:150-152˚C;IR(KBr)1260(p=O);1H-NMR(400MHz,CDCl3.)δ: 7.28(d, 8H, J=7.3Hz, Ph),4.49(d,4H,J = 13.2Hz,拱2.Ar), 4.00-3.85(m, 24H, OCH2.中国3.哟,2.中国2.中国3.),3.31(d,4H,J=13.2Hz,拱度2.1.97(qt,8H,J=7.0Hz,OCH2.中国2.中国3.), 1.21(t, 24H, J=7.0Hz, OCH2.中国3.), 1.00(t, 12H, J=7.0Hz, OCH2CH2CH3);色谱仪(100 mhz, CDCl3)δ: 159.6 (d, 4 jpc = 3.7赫兹), 134.6 (d、3 jpc = 14.7赫兹),132.2 (d, 2 jpc = 11 hz), 122.2 (d, 1 jpc = 191.2赫兹),77.2 (s), 61.9 (d, 2 jpc = 5.5赫兹),30.9 (s), 23.1 (s), 16.2 (d、3 jpc = 5.5赫兹),10.1 (s);31 P-NMR(160MHz的,CDCL3.)δ:13.7;MS(APCI,M + +1):1138。肛门:计算的。对于C56H84O16P4.: C, 59.15;7.45 H,。发现:C,59.23;H,7.59。 锥形-5,11,17,23-四(二异丙基膦)-25,26,27,28-四-n-丙氧基杯[4]芳烃[6b]: m、 p:153-155˚C;IR(KBr)1260(p=O);1H-NMR(400MHz,CDCl3)δ: 7.28 (d, 8 h, J = 13.3赫兹,Ph值),4.60 - -4.54 (m, 8 h, OCH (CH3.)2.),4.59(d,4H,J=12.7Hz,拱度2.a), 3.94(t, 8H, J=7.0Hz, OCH2.中国2.中国3.),3.32(d,4H,J = 12.7Hz,拱2.AR),2.00-1.93(M,8H,OCH2.中国2.中国3.), 1.27(d, 24H, J=6.0Hz, OCH(CH .3.)2.), 1.00(t, 12H, J=7.5Hz, OCH2.中国2.中国3.);13 C-NMR(100MHz的,CDCL3.)δ: 159.5(d, 4JPC=3.7Hz), 134.4(d, 3JPC=16.5Hz), 132.4(d,2JPC = 9.2Hz),122.8(d,1JPC = 95.6Hz),77.2(s),70.4(d,2JPC = 2.6Hz),31.2(s),24.0(s),23.8(S),23.8(S),23.1(s),10.2(S);31 P-NMR(160MHz的,CDCL3.)δ: 11.5;MS(APCI,M + +1):1250。肛门:计算的。对于C64H85O16P4.: C, 61.53;8.07 H,。发现:C, 61.45;H, 7。99。 23-Tetrakis Cone-5 11 17日(diphenyl-oxo-phosphino) -25年,26日,27日28-tetra-n-propoxycalix[4]芳烃(6 c): 国会议员:> 300˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ:7.42-7.21(M,48H中,Ph),4.53(d,4H,J = 13.2Hz,拱2.a), 3.94(t, 8H, J=7.3Hz, OCH2.中国2.中国3.),3.26(d,4 h, J = 13.2赫兹,拱门2.Ar), 1.98(qt, 8H, J=7.3Hz, OCH2.中国2.中国3.),0.99(T,12H,J = 7.3Hz,OCH2.中国2.中国3.);13 C-NMR(100MHz的,CDCL3.)δ:159.2134.8(d,3JPC=12.9Hz)、132.7(d,1JPC=103.0Hz)、132.7(d,2JPC=9.2Hz)、131.7(d,JPC=9.2Hz)、128.5(d,JPC=12.9Hz)、125.6(d,1JPC=106.6Hz)、77.1(s)、31.2(s)、23.1(s)、10.1(s);31 P-NMR(160MHz的,CDCL3.)δ: 22.3;女士(apci, M + + 1): 1394。肛门:计算的。对于C88H84O8.P4.: C, 75.85;6.08 H,。发现:C, 75.53;6.09 H,。 23-Tetrakis Partial-Cone-5 11 17日(diethylphosphono) -25年,26日,27日28-tetra-n-propoxy-calix[4]芳烃[7]: 国会议员:150 - 151˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ: 7.72 (d、2 h, J = 13.7赫兹,Ph值),7.61 (d, 2 h, J = 13.2赫兹,Ph值),7.41 (d, 2 h, J = 13.2赫兹,Ph值),6.98 (d, 2 h, J = 13.7赫兹,Ph值),4.28 - -3.38 (m, 30 h,拱门2.基于“增大化现实”技术,哟2.中国3.哟,2.中国2.中国3.), 3.21(d, 2H, J=13.2赫兹,拱2.Ar), 1.99-1.81(m, 8H, OCH2.中国2.中国3.),1.40(t,6H,J=7.0Hz,CH3),1.38(t,6H,J=7.0Hz,CH3),1.25(t,6H,J=7.0Hz,CH3),1.03(t,6H,J=7.0Hz,CH3),0.95(t,3H,J=7.0Hz,CH3),0.73(t,3H,J=7.0Hz,CH33.);13 C-NMR(100MHz的,CDCL3.)δ:160.9(S),160.1(S),159.4 (d, 4 jpc = 3.7 hz), 136.5 (d、3 jpc = 16.6赫兹),134.7 (d, 2 jpc = 11.0赫兹),133.9 (d、3 jpc = 16.5赫兹),133.6 (d, 2 jpc = 9.2赫兹),133.1 (d、3 jpc = 16.5赫兹),133.1 (d, 2 jpc = 11.0赫兹),132.9 (d, 2 jpc = 11.0赫兹),132.6 (d, 2 jpc = 11.0赫兹),121.8 (d、3 jpc = 16.6赫兹),122.7 (d, 1 jpc = 193.1赫兹),121.2 (d, 1 jpc = 194.8赫兹),121.0 (d, 1 jpc = 191.2赫兹),76.6,75.6,73.8,62.0 (d, 2 jpc = 5.5赫兹),61.8 (d, 2 jpc = 5.5赫兹),61.7 (d, 2 jpc = 5.5赫兹),61.6 (d, 2 jpc = 5.5赫兹),36.9,30.4,23.4,22.9,21.1,16.4,16.4,16.3,16.2,16.0,16.0,10.6,10.1,9.2 (s);31 P-NMR(160MHz的,CDCL3.)δ: 19.0, 18.6, 18.4;MS(APCI,M + +1):1138。肛门:计算的。对于C56H84O16P4.: C, 59.15;7.45 H,。发现:C, 59.32;7.49 H,。 部分锥-5,11,17,23-四(二异丙基膦)-25,26,27,28-四-n-丙氧基杯[4]芳烃[7b]: m、 p:125-128˚C;IR(KBr)1260(p=O);1H-NMR(400MHz,CDCl3.)δ: 7.69 (d、2 h, J = 13.7赫兹,Ph值),7.59 (d, 2 h, J = 13.2赫兹,Ph值),7.41 (d, 2 h, J = 13.2赫兹,Ph值),7.05 (d, 2 h, J = 12.2赫兹,Ph值),4.85 - -4.60 (m, 6 h, OCH (CH3) 2), 4.37 (m, 2 h, OCH (CH3.)2.), 4.14(d, 2H, J=13.2Hz,拱3.Ar), 3.87-3.75(m, 6H, ArCH2.基于“增大化现实”技术,哟2.中国2.中国3.), 3.63(t, 2H, J=8.0Hz, OCH2.中国2.中国3.),3.53-3.41(m,4H,OCH2.中国2.中国3.), 3.22(d, 2H, J=13.2Hz, ArCH .2.AR),1.96-1.74(M,6H,OCH2.中国2.中国3.), 1.40-1.20(m, 47H, OCH2.中国2.中国3., OCH(CH3)2), 1.01(t, 6H, J=7.3Hz, OCH2.中国2.中国3.), 0.92(t, 3H, J=7.3Hz, OCH2.中国2.中国3.), 0.75(t, 6H, J=6.0Hz, OCH(CH3.)2.);13 C-NMR(100MHz的,CDCL3.)δ: 160.6 (d, 4 jpc = 3.7赫兹),159.9 (d, 4 jpc = 3.7赫兹),159.3 (d, 4 jpc = 3.7赫兹),136.1 (d、3 jpc = 16.5赫兹),134.6 (d, 2 jpc = 9.2赫兹),133.9 (d、3 jpc = 16.6赫兹),133.3 (d, 2 jpc = 11.0赫兹),132年。8 (3 d, jpc = 16.5赫兹),132.8 (d, 2 jpc = 9.2赫兹),132.7 (d, 2 jpc = 11.0赫兹),132.6 (d、3 jpc = 16.6赫兹),124.2 (d, 1 jpc = 193.0赫兹),122.7 (d, 1 jpc = 194.8赫兹),76.5 (s), 75.5 (s), 73.3 (s), 70.4 (d, 2 jpc = 5.5赫兹),70.3 (d, 2 jpc = 5.5赫兹),70.2 (d, 2 jpc = 5.5赫兹),70.0 (d, 2 jpc = 5.5赫兹),37.2 (s), 30.6 (s), 24.1 (s), 24.0 (s), 23.9 (s), 23.1 (s), 23.1 (s), 22.6 (s), 20.9 (s), 10.6 (s), 10.3 (s),9.4 (s);31 P-NMR(160MHz的,CDCL3.)δ:12.8,12.3,11.9;MS(APCI,M + +1):1250。肛门:计算的。对于C64H85O16P4.:C,61.53;H,8.07。发现:C,61.65;H,8.25。 23-Tetrakis Partial-Cone-5 11 17日(diphenyl-oxo-phosphino) -25年,26日,27日28-tetra-n-propoxycalix[4]芳烃c [7]: 国会议员:186 - 188˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ: 7.77 - -7.72 (m, 4 h, Ph值),7.58 - -7.25 (m, 42小时,Ph值),7.15 (d, 2 h, J = 11.7赫兹,Ph值),4.17 (d, 2 h, J = 12.7赫兹,拱门2.AR),3.74点(s, 4 h,拱门2.的Ar),3.57(T,4H,J = 8.0Hz,OCH2.中国2.中国3.),3.46(t,4H,J=8.0Hz,OCH2.中国2.中国3.),3.43(T,4H,J = 8.0Hz,OCH2.中国2.中国3.), 3.16(d, 2H, J=12.7Hz, ArCH2Ar), 1.59-1.53(m, 6H, OCH2CH2CH3), 1.26-1.22(m, 2H, OCH2.中国2.中国3.), 0.90-0.80(m, 9H, OCH2.中国2.中国3.),0.52(t,3H,J=7.6Hz,OCH2.中国2.中国3.);13 C-NMR(100MHz的,CDCL3.)δ: 160.9(d, 4JPC=3.7Hz), 159.5(d, 4JPC=4.3Hz), 136.5(d, 3JPC=12.9Hz), 135.0(d, 2JPC=11Hz), 134.0(d, JPC=12.9Hz), 133.6, 133.5, 133.4, 133.3, 133.2, 133.1, 133.1, 132.9, 132.9, 132.8, 132.4, 132.1, 132.0, 131.9, 131.8, 131.7, 131.6, 128.7, 128.6, 128.5, 128.4, 128.4, 128.4, 128.2, 126.9 (d, 1 jpc = 104.8赫兹),124.7 (d, 1 jpc = 108.4赫兹),124.4 (d, 1 jpc = 108.4赫兹),76.5,75.3,74.2,37.4,31.5,31.0,23.2,23.1,22.6,21.3,14.1,10.3,9.6 (s);31 P-NMR(160MHz的,CDCL2.)δ:23.2,22.6,22.3;毫秒(apci,M++1):1394。肛门:计算的。对于C88H84O8.P4.: C, 75.85;6.08 H,。发现:C, 76.06;5.98 H,。 圆锥-5,11,17,23- tetrakis (diethylphosphono)-calix[4]arene Bis(crown ether) [8a]: 国会议员:231 - 232˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ: 7.46 (d, 4 h, J = 11.2赫兹,Ph值),7.43 (d, 4 h, J = 11.2赫兹,Ph值),5.16 (d, 2 h, J = 12.2赫兹,拱门2.Ar), 4.52(d, 2H, J=12.2Hz, ArCH2.Ar), 4.35(d, 4H, J=10.7Hz, OCH2.中国2.O), 4.35 (s, 4 h,OCH2.中国2.中国3.), 4.24(s, 4H, J=10.7Hz,OCH2.中国2.O) ,4.01-3.86(米,20小时,赭石)2.中国2.啊,呀2.中国3.), 3.37(d, 2H, J=12.2Hz, ArCH .2.的Ar),3.32(d,2H,J = 12.2Hz,拱2.Ar), 1.16-1.11(m, 24H, OCH2.中国3.);13 C-NMR(100MHz的,CDCL3.)δ:158.7(d,4JPC = 3.7Hz),135.5(d,3JPC = 16.5Hz),135.3(d,3JPC = 16.5Hz),132.9(d,2JPC = 11.0Hz),132.0(d,2JPC=11.0Hz),123.6(d,1JPC=123.6Hz),76.3(s),73.9(s),62.0(s),30.5(s),29.7(s),16.1(d,3JPC=3.7Hz);31P-NMR(160MHz,CDCl3.)δ: 13.2;女士(apci, M +): 1109。肛门:计算的。对于C52H72O18P4.值:C,56.32;H,6.54。实测值:C,56.55;H,6.49。 圆锥-5,11,17,23- tetrakis (diisopropylphosphono)-calix[4]芳烃 国会议员:185 - 186˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ:7.43(d,4H,J=13.2Hz,Ph),7.42(d,4H,J=13.2Hz,Ph),5.15(d,2H,J=12.7Hz,拱度2.Ar), 4.58-4.50(m, 10H, ArCH2.基于“增大化现实”技术,OCH (CH3.)2.),4.35(d,4H,J = 11.2Hz,OCH2.中国2.O), 4.24(d, 8H, J=5.4Hz, OCH2.中国2.O), 3.87(m, 4H, OCH2.中国2.O), 3.36(d, 2H, J=12.7Hz, ArCH2.Ar), 3.30(d, 2H, J=12.2Hz, ArCH2.Ar),1.25(d,12H,J=6.0Hz,OCH(CH3.)2.), 1.23(d, 12H, J=6.0Hz, OCH(CH .3.)2.),1.09(d,12H,J=6.0Hz,OCH(CH3.)2.),1.05(d,12H,J = 6.0Hz,OCH(CH3.)2.);13 C-NMR(100MHz的,CDCL3.)δ: 158.5 (d, 4 jpc = 3.7赫兹),135.2 (d、3 jpc = 16.6赫兹),135.0 (d、3 jpc = 16.6赫兹),132.8 (d, 2 jpc = 11 hz), 132.0 (d, 2 jpc = 11 hz), 125.1 (d, 1 jpc = 193 hz), 76.2 (s), 73.9 (s), 70.5 (d, 2 jpc = 5.5赫兹),30.7 (s), 29.8 (s), 23岁。9(s),23.8(d,3JPC=3.7Hz),23.7(d,3JPC=3.7Hz);31P-NMR(160MHz,CDCl3.)δ:11.1;MS(apci,M++1):1221。肛门:计算的。对于C60H84O18P4.: C, 59.01;7.26 H,。发现:C, 58.93;7.19 H,。 锥形-5,11,17,23-四(二苯基氧基膦)-杯[4]芳烃双(冠醚)[8c]: 国会议员:187 - 189˚C;红外(KBr) 1260 (P = O);1 H-NMR(400MHz,CDCL3.)δ: 7.45 - -7.22 (m, 48 h, Ph值),5.22 (d, 2 h, J = 12.2赫兹,拱门2.Ar), 4.55(d, 2H, J=12.2Hz, ArCH2.Ar), 4.35(d, 4H, J=10.8Hz, OCH2.中国2.O), 4.24(d, 8H, J=4.9Hz, OCH2.中国2.O), 3.89-3.84(m, 4H, OCH2.中国2.O), 3.27(d, 2H, J=12.2Hz, ArCH .2.Ar), 3.23(d, 2H, J=12.2Hz, ArCH2.AR);13 C-NMR(100MHz的,CDCL3.)δ: 158.4 (s), 135.6 (d、3 JPC = 12.9赫兹),135.4 (d、3 JPC = 12.9赫兹),133.1 (d, 2 JPC = 11 hz), 132.3 (d, 1 JPC = 117.7赫兹),132.2 (d, 2 JPC = 11 hz), 131.8 (s), 131.6 (s), 131.5 (s), 128.5 (d, JPC = 14.7赫兹),126.9 (d, 1 jpc = 104.8赫兹),76.2 (s), 73.7 (s), 69.3 (s), 30.7 (s), 29.9 (s);31 P-NMR(160MHz的,CDCL3.)δ: 23.1;女士(apci, M + + 1): 1366。肛门:计算的。对于C84H72O10P4.: C, 73.89;5.32 H,。发现:C, 74.13;5.69 H,。 萃取性杯[4]芳烃5,6,7,和8对各种金属氯化物采用双层体系测定5、6、7和8杯[4]芳烃对各种金属氯化物的萃取率,方法如下-3)和含有4n -盐酸和0.1 mmol dm的水溶液(20 ml)-3在30˚C磁搅拌20h。提取上层水溶液中的一部分,用电感耦合等离子体发射光谱法进行分析。在没有任何样品的情况下进行了类似的提取实验。可萃取性是通过下面的公式的装置的在水溶液中的金属氯化物的浓度的基础上确定: 可提取性(%)=[(A0- a) / a0]x100 一个0和A分别为样品不存在(初始浓度)和存在(最终浓度)时金属氯的水溶液浓度。 配合物的分离与性质在杯[4]芳烃6c和FeCl3之间杯[4]芳烃6c与FeCl之间的配合物3.成功地从用于提取实验的双层氯仿溶液中分离出来。,并进行了光谱(UV和31P-NMR)、电化学(循环伏安法)和mp测量。 结果与讨论四溴环[4]芳烃衍生物1-4{1(R=Me-paco(=部分锥)18),2(R=n-Pr-cone),3(R=n-Pr-paco),4(R=-CH2.中国2.OCH2.中国2.- -cone)}的制备方法与文献报道的方法一致。1.5.,19,20 Arbuzov reaction of tetrabromocalix[4]arene tetra-n-propylether 2 (cone ) and 3 (paco) with trialkyl phosphite ( P(OR)3.)或乙基二苯基次膦(PH2.P(OEt))使用NiBr2.作为路易斯酸催化剂,在180˚C的苯腈中顺利地进行了相应的新杯[4]芳烃6a-c (cone)和7a-c (paco),具有二烷基膦酸酯(PO(OR))。2.)或二苯基氧化膦(Ph2.PO)基团在每一个以优良产率(51〜97%)中的苯环的对位,在表1中,如图所示。 表1。Arbuzov反应合成四膦基杯[4]芳烃衍生物。 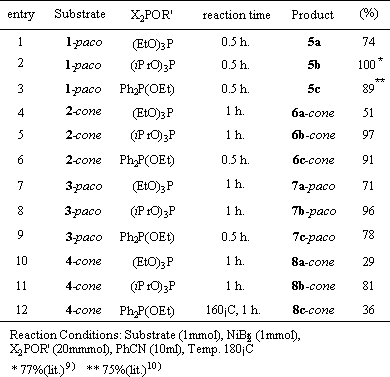
以具有二甘醇基的四溴杯[4]芳烃4 (cone)为原料,与P(OEt)反应,低收率得到了杯[4]芳烃8a (cone)和8c (cone)。3.和Ph值2.P(OET),而4(浓)用P上的反应(O我Pr)3.给出了相应产品8b(锥体)的81%收率。 杯[4]芳烃5、6、7和8对各种金属氯化物的萃取性测量如下。双层由1.0 mmol dm的氯仿溶液组成-35-8和含有0.1 mmol dm的4n -盐酸水溶液-3金属氯化物,在30℃磁力搅拌20小时。然后金属氯化物在上部水溶液的等分试样的水浓度是通过电感耦合等离子体(ICP)发射光谱法进行分析。 结果表明,具有4个二烷基膦酸酯基团的杯[4]芳烃5a,b, 6a,b, 7a,b和8a,b对FeCl等金属盐均无萃取性3., CoCl2., NiCl2., ZnCl2.和LaCl3..而含有氧化基团5c、6c、7c和8c的化合物仅对FeCl表现出高度选择性和优异的萃取行为3.即使在含有相同浓度的各种金属氯化物(FeCl)的水溶液中3., CoCl2., NiCl2., ZnCl2.),见表3。 表2。杯[4]芳烃衍生物的P-NMR谱。 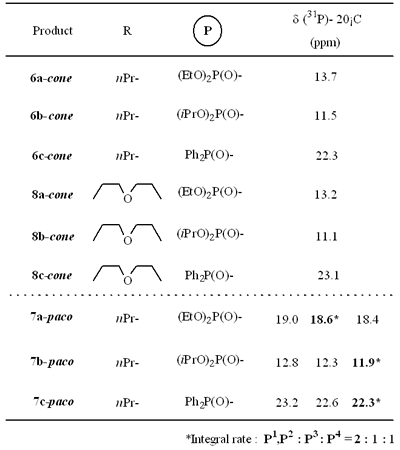
也许还值得注意,一个6 c与四氧化diphenylphosphine组织显示,5 c中可萃取性最高,6 c, 7和8 c,可能是因为丙醚组较低的边缘使构象更加严格和孔尺寸更适合[FeCl4.-,如表3和表4所示。 表3。提取FeCl3.在与杯[4]芳烃衍生物5c-8c和7a,b。
|
1. |
5度 |
28 |
0.1 |
0 |
0 |
0 |
2. |
6摄氏度 |
80 |
1.0 |
0.2 |
0.7 |
0 |
3. |
7 c |
67 |
0.9 |
0 |
1.1 |
0 |
4. |
8 c |
46 |
1.0 |
0.8 |
0.7 |
0 |
5. |
7一个 |
0 |
0 |
0 |
0 |
0 |
6. |
7 b |
0 |
0 |
0 |
0 |
0 |
表4。提取FeCl3.与竞技场杯和TPPO混合溶液
|
1. |
5度 |
FeCl3. |
4 N |
48 |
2. |
6摄氏度 |
FeCl3. |
4 N |
92 |
3. |
7 c |
FeCl3. |
4 N |
79 |
4. |
8 c |
FeCl3. |
4 N |
69 |
5. |
7 b |
FeCl3. |
4 N |
0 |
6. |
TPPO2. |
FeCl3. |
4 N |
0 |
1.提取条件:[有机相]:1mM-CHCl3., 20ml[水相]:0.1mM的FeCl3., 20ml, c[HCl]: 4N, 20h, 30jC
2.TPPO:三苯基膦氧化物 此外,三苯基氧化膦(TPPO)未显示(条目4)的提取物的条件下的任何萃取性,这指示的杯[4]芳烃的具体结构特征。 它是很有趣带来的FeCl在萃取性(E%)逐渐增加的双层体系的水溶液的pH值增加3.如图2所示,当使用8N-HCl作为萃取剂时,提取率几乎达到100%。 ![AZoJomo - AZO Materials Journ欧洲杯足球竞彩al of Online - Extraction of FeCl3 by HCl Concentration Change for Calix[4]arene 6c](//www.wireless-io.com/work/3td2qTvKNU9g4UBLjUEg_files/image004.gif)
图2。提取FeCl3.通过HCl浓度的变化对杯[4]芳烃6c。 此外,白色固体从通过提取在双层系统中的有机层中使用的杯[4]芳烃6C具有四个二苯基膦氧化物基团分离显示特有的电化学和光谱行为。因此,固体节目熔点在80-81°(mp of 6c: >300 .°), 和在小但特征吸收λ马克斯:在它的紫外线光谱370纳米。杯[4]芳烃6c和固体展示在分别-1.43 V和-1.92 V(相对于Ag / Ag +)会,它们的还原电位,在它们的环状体积安培法,在δ=41.2 ppm,而6c为单线态峰δ= 22.3 ppm。 从萃取行为和特征性质的实验结果来看,该固体似乎由杯[4]芳烃6c和FeCl之间的络合物组成3.,如图3所示,其中四个二苯基氧化膦基团的氧原子被质子化,一个FeCl分子4.阴离子包含在一个阳离子腔中,被四个6c的二苯基膦氧化物基团包围。锥状构象和下缘的四个Oi-Pr基团可能是产生fel客体分子合适大小的空腔的原因4.阴离子。 ![AZoJomo-AZO材料在线杂志-杯[4]芳烃6c和Fe欧洲杯足球竞彩Cl3之间的复合体](//www.wireless-io.com/work/3td2qTvKNU9g4UBLjUEg_files/image005.gif)
图3。杯[4]芳烃6c与FeCl之间的配合物3. 作为结论,新颖杯[4]芳烃衍生物轴承上的每个的四个苯环6c中,7c的对位二苯基膦氧化物基团,和8c是通过tetrabromocalix的Arbzov反应合成[4]芳烃衍生物用乙酸乙酯二苯基次膦保持各原构。他们都表现出高选择性,只针对大能力的离子对提取的FeCl3.,而在边缘具有四个正丙基的6c显示出最高的可萃取性。 
图4。Arbuzov反应。 确认本研究由21世纪COE计划和日本文部科学省重点领域科学研究资助项目(No. 13029038)资助。欧洲杯线上买球 引用和笔记1.C. D. Gutshe,“杯芳烃:超分子化学专论”,(1989)1,英国皇家化学学会,剑桥。 2.C.D.Gutsche,B.Dhawan,J.A.Levine,K.H.No和L.J.Bauer,“杯芳烃9杯[4]芳烃醚和酯的构象异构体”,四面体,39 3,(1983)409-426。 3.诉玻姆,“杯芳烃,具有(几乎)无限可能性的宏观循环”,安新。化学。Int。艾德,心血管病。, 34(1995) 713-745。 4.兆。6 . Chang and I. Cho,“Synthesis of New Metal阳离子- selective Ionophores from杯芳烃:Synthesis and ionic binding Properties”,J. Chem. J. Chem. (sci)。Soc。陈志强,(1986)。 5.A. Ikeda和S. Shinkai,“1,3- alternate - calix[4]芳烃的异常高离子光性:在阳离子的络合Π捐助者参与?”,四面体。, 33, 48,(1992) 7385-7388。 6.M. Takeshita, S. Shinkai,“杯芳烃功能化和识别能力的最新研究:第三宿主分子”,Bull.Chem.。Soc.Jpn.,68(1995)1088-1097。 7.K.本岛,H.早川T.北川和Y.山本,“分离和分析由有机试剂”,石BUNSEKI讲座6,共立出版,(1964)。 8.F. Diederrich和P. J.斯唐编, “MATAL催化的交叉偶联反应”,WILEY-VCH,(1977)。 9.V.I.Malchenko、L.I.Atamas、V.V.Pirozhenko和L.N.Markovsky,Zh.Obshch.Khim.,62(1992)2623-.2625。 10.S. Ozegowski, B. Costisella and J. Gloede,“Selektive Einführung von phospylgruppen am ' Upper Rim ' von Calix[4]arenen Synthese und NMR-Untersuchungen”,磷、硫和硅,119(1996)207 -223。 11.田文华,“一种新型杯芳烃的液-液萃取及其对碱金属阳离子的影响”,《化学学报》。摩尔。Recogn。, 10(1991) 57-61。 12.此外,还对具有部分功能基团作为膦酸酯基团与苯环之间的间隔基团的杯[4]芳烃进行了化学(合成、构象分析和性质)研究。看到引用13 - 14日。 13.J. F. Malone, D. J. Marrs, M. A. McKervey, P. O 'Hagan, N. Thompson, A. Walker, F. arnau - neu,o . Mauprivez蔡明俊。Schwing-Weill,肯尼迪。12 . dool, H. Rouquette和n . Simon,《杯[n]芳烃膦氧化物》。核废料处理中萃取铕、钍、钚和镅的新型阳离子受体”,化工学报。 14.A. Arduini, V. Böhmer, L. Delmau, j.f.Desreux,肯尼迪。M. A. G. Carrera, B. Lambert, C..Musigmann, A. Pochini, A. Shivanyuk和F. Ugozzoli,“刚性杯芳烃轴承四。Carbamoylmethylphosphineoxide或。氨基甲酰基磷酸化在广泛的功能。边缘”,化学。欧元。[J]。 15.M. Almi, A. Arduini, A. Casnati, A. Pochini和陈志强,“杯芳烃的氯甲基化和水溶性大环主体的合成”,高分子材料学报,45,7(1989)2177-2182。 16.陈志强,“溴代25,26,27,28-四丙氧基杯[4]芳烃的选择性卤素-锂交换反应”,化学学报。化学。, 61(1996) 6651-6655。 17.F. Hamada, S. G. Bott, G. W. Orr和A. W. Coleman,“Thiocalix[4]芳烃。1 .乙硫杯[4]芳烃甲基醚的合成与结构及溴杯[4]芳烃甲基醚的相关结构, 9(1990) 195-206。 18.“离子模板对杯芳烃构象的影响”,《化学学报》。化学。, 56(1991) 295-300。 19.圆锥为圆锥构象,paco为部分圆锥构象。 20.c.d. Gutsche和p.f. Pagoria, " Calixarenes. "16.功能化杯芳烃:直接取代途径”,J. Org。化学。, 50(1985) 5795-5802。 21.a . Soi w·鲍尔h .毛瑟枪,c·摩尔·f·Hampel和a . Hirsch”调查的动态属性25日26日27日28-Tetraalkoxycalix[4]芳烃:Para-substituent帕科- Solvent-dependent性质的矫形器的热力学参数和决心捏Conelpinched锥转换”,j .化学。Soc。《中国科学院大学学报(自然科学版)》1998年第2期。 联系方式 |