2010年4月28日
洗碗时弹出气泡,当肥皂球形成时,您可能会释放几滴水被困。几年前,国家标准技术研究所(NIST)马里兰州大学(UM)使用微观流体(微流体)设备开创了一种方法*,该设备利用相同的原理来创建来自磷脂的液态囊泡,这是磷脂,这是动物细胞膜的基本块,是脂肪复合物。
这些结构被重视,因为它们的潜在用途将药物直接传递给体内的癌症和其他疾病细胞。
脂质体广泛应用作为人造药物载体受到许多限制因素的阻碍,例如大小,结构不稳定和高生产成本的不一致。在一项新研究中,** NIST和UM研究人员详细介绍了其脂质体制造技术的运行方式,该技术如何称为受控的微流体混合和纳米颗粒确定的命令,以最大程度地提高其有效性。他们的目标是更好地理解命令的工作原理,因为它产生脂质体,其直径从约50至150纳米(十亿分之一的仪表)控制,它们的尺寸始终均匀,并且在可能被称为“装配线”中产生的廉价且廉价地产生。a-microchip。”
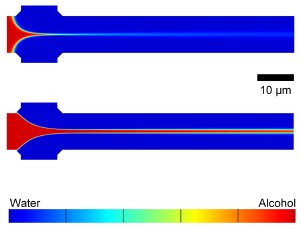 计算机模拟显示了指挥微流体设备中水和异丙醇的混合。酒精将与溶解的凤凰混合在运行中,从左侧到右侧的中心入口流动,并由从顶部和底部入口流入的水聚焦。调节流速可将聚焦的流(顶部)或更宽(底部)产生控制,从而控制脂质体大小。信用:NIST
计算机模拟显示了指挥微流体设备中水和异丙醇的混合。酒精将与溶解的凤凰混合在运行中,从左侧到右侧的中心入口流动,并由从顶部和底部入口流入的水聚焦。调节流速可将聚焦的流(顶部)或更宽(底部)产生控制,从而控制脂质体大小。信用:NIST
研究人员通过将微小的通道蚀刻到硅晶片中,以制造相同的技术来制作集成电路。在指挥官中,通过中央入口通道喂入溶于异丙基醇的磷脂分子被水基溶液喂入“混合器”通道中,并“聚焦”到流体射流中(在生产中会携带囊泡的药物或其他货物)通过两个侧通道添加。这些成分通过在流动流体流的界面扩散而混合在一起时将它们混合在一起,将磷脂分子引向自组装到受控大小的纳米级囊泡中。测试了不同的微流体设备设计和流体流量条件,以研究它们在产生脂质体中的作用。
研究小组发现,他们的脂质体制造过程从根本上取决于流体流的流量和混合。可以通过操纵流体流速来“调整”脂质体的大小,该流动速与微流体设备的尺寸结合使用,可以确定所得的混合条件。以缓慢的速度流动的磷脂液含量紧密聚焦的流倾向于在混合通道的开头和形成小囊泡的开始时迅速与缓冲液混合。以快速速度流动的松散聚焦的流沿较远的混合通道的长度传播,从而使更多的混合时间并产生较大的囊泡。
研究人员指出,通道的几何形状在调节生产速度以及生产脂质体的数量和浓度方面起着额外的作用。这对于脂质体的未来临床应用以及将命令集成到更复杂的医疗保健系统中可能很重要。
* A. Jahn,W.N。Vreeland,M。Gaitan和L.E.locascio。在微流体通道中以流体动力焦点进行的受控囊泡自组装。美国化学学会杂志。卷。126,2674-2675(2004年2月17日)。
** A. Jahn,S.M。Stavis,J.S。Hong,W.N。Vreeland,D.L。Devoe和M. Gaitan。微流体混合和纳米级脂质囊泡的形成。ACS纳米。2010年3月31日在线发布。