2010年7月5
Biomerix公司今天宣布,它已收到美国食品和药物管理局(FDA) 510 (k)间隙市场Biomerix腹疝
维修网,最新的除了其创新组合的软组织修复设备。Biomerix腹疝修补术的网,两个截然不同,是第一个也是唯一设备以Biomerix生物材料™一方面,旨在促进组织的生成,以及resorbable保护膜另一方面,旨在减少组织对设备直接接触的内脏。表示用于疝和软组织不足和临时连接筋膜的缺陷。
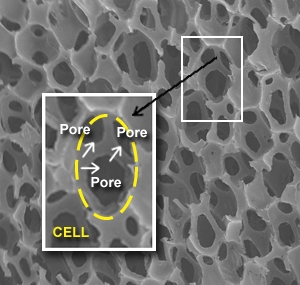 Biomerix生物材料™
Biomerix生物材料™
有超过400000人患有腹疝今天在美国。腹疝是腹部肿块,通常是一个组织膨胀或小面积的肿胀。腹疝也称为一个切口疝,因为它可以发生在任何之前手术切口。人口老龄化和越来越多的肥胖病人是导致腹疝发病率的上升。当前的产品解决方案无法解决高复发率和粘连形成的风险通常与腹疝修补术有关。Biomerix腹疝修补术的网状构造支持组织的生成。最先进的设计提供了一种resorbable保护膜一侧作为屏障,减少粘连到设备的风险。通过整合Biomerix生物材料™平台,腹疝修补网的柔软和柔软设计提供了严重的外科医生一致性能在开放和腹腔镜手术。
“FDA批准Biomerix腹疝修补网代表了下一代在腹侧和切口疝修复假体。我们认为这部小说Biomerix生物材料理想的支架特性导致成功修复的结果,使它成为引人注目的替代其他合成生物材料,”肯尼斯·g·海耶斯,Biomerix公司的总裁兼首席执行官。欧洲杯足球竞彩
来源:http://www.biomerix.com/