2016年8月25日
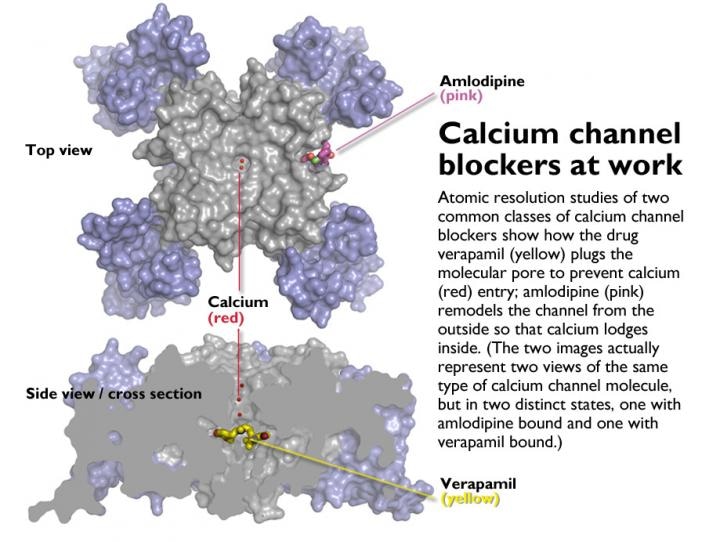 对两种常见的钙通道阻滞剂的原子分辨率研究,一种治疗不规则心跳,另一种控制高血压和心绞痛。图片来源:卡特罗尔和郑实验室/华盛顿大学
对两种常见的钙通道阻滞剂的原子分辨率研究,一种治疗不规则心跳,另一种控制高血压和心绞痛。图片来源:卡特罗尔和郑实验室/华盛顿大学
两种特定的钙通道阻滞剂,通常用于心脏病患者,根据它们在钙通道分子上不同部位的作用而产生不同的治疗效果。这一发现是通过原子水平分析得出的。
世界各地的患者通过服用钙通道阻滞剂来控制心血管问题。
最新一期的《自然》在线高级版刊登了一项研究,研究人员解释了这些药物的两种不同化学类别的基本作用模式是如何不同的。这一知识是通过检查它们结合位点的原子结构获得的。
该项目由威斯康辛大学医学威廉·a·卡特拉尔(William A. Catterall)博士,华盛顿大学药理学教授和霍华德·休斯医学研究所研究员,郑宁(Ning Zheng),华盛顿大学药理学教授。华盛顿大学药理学博士后研究科学家唐林是《自然》杂志报告的第一作者。
钙通道阻滞剂首次被发现并作为药物被批准是在前半个世纪。这些阻滞剂已经成为心血管疾病的理想治疗方法。
最近的研究结果可以为设计更好、更安全的钙通道阻滞剂提供信息,以控制高血压、胸痛和心律失常。
用于治疗心律失常的钙通道阻滞剂(如维拉帕米)与用于治疗高血压或心绞痛的钙通道阻滞剂(如氨氯地平)进行了比较。
地尔硫卓和第三类钙通道阻滞剂可以降低心率和扩张血液。这些药物在本研究中未被考虑。
研究人员专注于研究钙通道阻滞剂分子如何与钙通道协同工作,钙通道是控制钙离子通过细胞膜的分子孔。
心肌细胞或静脉和动脉中的平滑肌细胞的毛孔打开,导致钙离子涌入细胞,促使心脏泵血,动脉收缩,缩小直径,从而增加血压。
通过干扰这些分子孔,钙通道阻滞剂可以抑制一种主要的强大的心血管反应,这种反应可能导致高血压或不规则的心脏跳动。
药理学家认为,类似维拉帕米的药物能够在物理上阻断钙通道毛孔,以阻止钙进入细胞,恢复正常的心率。然而,类似氨氯地平的药物——也被称为二氢吡啶——被认为间接地阻止钙通道激活和孔隙打开,从而预防心绞痛和高血压。
然而,这些不同的行动机制背后的具体结构仍然是未知的。
x射线晶体学有助于确定巨大蛋白质分子中原子的排列。x射线晶体学和离子通道功能分析的进展,目前使研究人员能够研究药物作用的亚分子深度。
研究人员观察了药物分子与钙通道结合的位置,以及这种结合如何改变通道的功能。
心绞痛药物氨氯地平与血压的结合点被确定为钙通道分子的外边缘。位于中心孔周围的电压传感器对电势很敏感。
结合位点位于钙通道分子四个亚基中的两个之间的中心孔结构的外侧。这种结合通过改变通道的形状和在通道内永久放置一个钙离子来关闭通道。
氨氯地平会巧妙地重塑小孔,这样钙离子就会被拉到一边,一直粘在那里,就像被锁住了一样。
郑宁,华盛顿大学教授
相比之下,维拉帕米分子有可能堵塞钙通道的中央腔,直接阻断钙离子传导途径。
在心悸时,维拉帕米利用钙通道的复发开口,就像心房扑动或心房颤动时一样。频繁打开毛孔增加了维拉帕米分子滑进中央腔并封闭毛孔的机会。
维拉帕米似乎能更好地与心脏快速跳动部位的钙通道结合,并减慢它们的速度。
威廉·a·卡特罗尔博士,华盛顿大学研究员
他强调,Bertil·希勒,他的威斯康辛大学的同事和生理学和生物物理学教授和他的同事之前说明快速发射频率的影响钠离子通道封锁在他们研究处理局部麻醉药物,如利多卡因用于预防外科,牙科疼痛。
血管细胞中的钙通道在静息状态下通常是封闭的。氨氯地平分子调节钙通道的电压依赖性激活,而不依赖于通道的反复打开以进入孔。
这就是为什么有助于放松血管的类氨氯地平药物能够治疗高血压和心绞痛的挤压性紧痛,而对心脏本身没有重大影响的原因。这将它们与类似维拉帕米的药物区分开来,后者支持心脏电回路中活跃细胞中的钙通道。
通过了解两个结合位点的相关细节,可以开发出精确匹配的钙通道阻滞剂。更精确的形状还可以防止下一代阻滞剂无意中将自己定位在错误的结合位点上,从而产生不必要的副作用。
钙通道阻滞剂是相对安全的药物,Catterall解释说,“但过量服用会引起毒性,导致室性心律失常或心脏或平滑肌细胞收缩过度抑制。”
他接着说,基于结构的、增强的药物设计可能为小而有效的药物剂量腾出空间,这些药物剂量更安全、更具体。例如,改变药物设计可以防止另一个可能导致不必要副作用的因素。钙通道阻滞剂对钠通道的脱靶阻断。
这项新研究是以细菌离子通道为基础的,已知细菌离子通道是包括人类、鱼类、苍蝇和蠕虫在内的其他生命形式的钙和钠通道的祖先。
这些古老的细菌通道仍然能够识别为人类设计的药物。我们的第二作者Tamer Gamal El-Din(药理学代理助理教授)所做的实验表明,这些药物对细菌通道的作用与它们对哺乳动物的作用相同。值得注意的是,最基本的细菌通道对这些治疗心律失常和某些其他心血管疾病的现代药物有反应。
威廉博士米一个。Catterall华盛顿大学研究员
这项研究得到了联邦政府资助的劳伦斯伯克利国家实验室先进光源的资助,在那里可以检测未结合和结合的钙通道的微小结构。
有趣的是,郑解释说,在加州的同步加速器束流线上进行的实验,可以在西雅图的华盛顿大学通过一个简单的笔记本电脑进行远程操作,由林堂(Lin Tang)和参与这项研究的其他研究人员操作。
该项目的其他研究人员包括华盛顿大学药理学博士候选人Teresa M. Swanson;David C. Pryde,英国辉瑞全球药物化学研究中心;以及华盛顿大学药理学研究教授Todd Scheuer。
这个刊登在最新一期《自然》杂志上的项目得到了美国国立卫生研究院国家心肺和血液研究所(授权R01 HL112808)、国家研究服务奖(授权T32GM008268)和霍华德休斯医学研究所的支持。