2018年1月4
从理论上讲,克里斯托弗·沃尔弗顿(Christopher Wolverton)的超富锂电池似乎不应该工作。首先,这种新型电池利用了铁,而铁在电池中是出了名的失效。此外,电池利用氧气来帮助驱动化学反应,研究人员最初认为这将导致电池变得不稳定。然而,它已经导致了一个更高容量的电池,工作非常好。
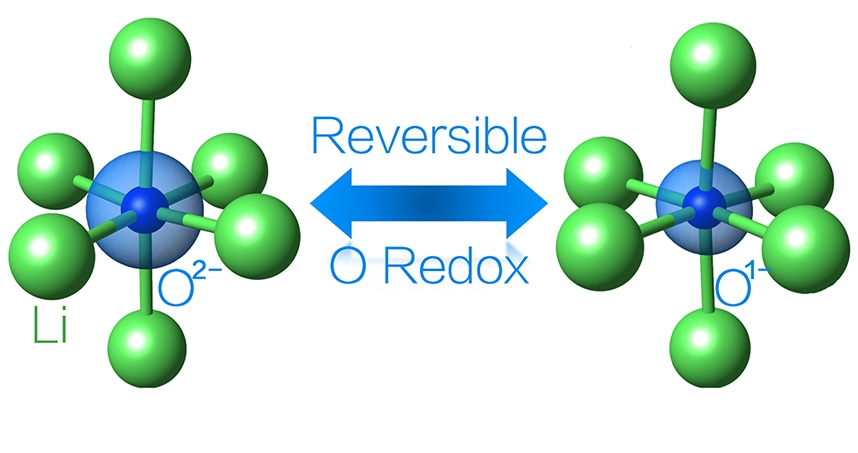 图片来源:西北大学
图片来源:西北大学
沃尔弗顿的团队与阿贡国家实验室的研究人员合作,成功地开发了一种可充电的锂-铁-氧化物电池,它比普通的锂-钴-氧化物电池能循环更多的锂离子。
其结果是一个更大容量的电池,有可能使电池驱动的汽车和智能手机使用更长时间。
“我们对这种电池反应的计算预测非常令人兴奋,但如果没有实验证实,将会有很多怀疑论者,”沃尔弗顿说欧洲杯足球竞彩欧洲杯线上买球西北大学麦考密克工程学院.“事实上,它确实有效,这是了不起的。”
这项研究得到了美国能源部能源前沿研究中心项目的支持,最近在《华盛顿邮报》上发表自然能源.伍尔弗顿实验室的博士生姚振鹏和阿贡大学的博士后詹春是这篇论文的第一批作者。Argonne负责实验部分的研究,Wolverton和Yao负责计算开发。
锂离子电池的功能是在负极和负极之间来回移动锂离子。当电池充电时,离子会回到阳极,并储存在那里。阴极是由过渡金属、锂离子和氧组成的化合物制成的。过渡金属通常是钴,当锂离子从阳极到阴极然后再返回时,它能有效地储存并释放电能。阴极的容量随后受到过渡金属中能够参与反应的电子数量的限制。
在传统情况下,过渡金属进行反应.因为每一个钴只有一个锂离子,这限制了可存储的电荷量。更糟糕的是,目前手机或笔记本电脑的电池通常只使用阴极中的一半锂。
克里斯多夫教授Wolverton
20年来,锂钴氧化物电池已经商业化,但研究人员长期以来一直在寻找更高容量、更便宜的替代品。沃尔弗顿的团队通过两种策略改进了普通的锂钴氧化物电池:迫使氧气参与反应过程和用铁取代钴。
如果氧气也能储存和释放电能,那么电池将有更大的容量来储存和使用更多的锂。尽管其他研究小组过去也尝试过这种方法,但只有少数人成功了。
“以前的问题通常是,如果你试图让氧气参与反应,化合物会变得不稳定,”姚明说。“氧气会从电池中释放出来,使反应不可逆。”
沃尔弗顿和姚使用计算方法发现了一个可以可逆工作的公式。他们首先用铁取代钴,这是有益的,因为它是元素周期表上最便宜的元素之一。通过计算,他们发现了锂离子、铁离子和氧离子的正确平衡,从而阻止氧气逸出,使铁和氧同时驱动可逆反应。
“电池不仅有一种有趣的化学反应,因为我们从金属和氧中获得电子,而且我们使用铁,”Wolverton说。“这有可能制造出更便宜的更好的电池。”
另一个重要方面是,完全可充电电池从四个锂离子开始,而不是一个。目前的反应能够可逆地利用其中一个锂离子,主要是增加现有电池的容量。然而,通过使用氧和铁来驱动反应,使四种元素来回循环的潜力确实是诱人的。
“每种金属有四个锂离子——这将改变一切,”Wolverton说。“这意味着你的手机可以使用8倍的时间,你的汽车可以行驶8倍的距离。如果电池驱动的汽车在续航里程和成本上能与汽油驱动的汽车竞争,甚至超过汽油驱动的汽车,那将改变世界。”
沃尔弗顿已经向西北大学创新与新投资办公室申请了这种电池的临时专利。接下来,沃尔弗顿和他的团队计划发现这种策略可以发挥作用的其他化合物。